1ª Atualização Anual da Lista de Medicamentos Críticos
Foi publicada a 1ª atualização anual da lista de medicamentos críticos da União Europeia, no passado dia 12 de dezembro de 2025.
A Agência Europeia de Medicamentos (EMA), em articulação com os Chefes das Agências de Medicamentos (HMA) e a Comissão Europeia, publicou este instrumento fundamental para prevenir ruturas de abastecimento e garantir a disponibilidade de medicamentos essenciais na UE, reforçando uma abordagem coordenada e preventiva entre as autoridades reguladoras.
A lista inclui medicamentos de uso humano considerados essenciais para o bom funcionamento dos sistemas de saúde, abrangendo medicamentos inovadores e genéricos, em áreas como vacinas, doenças raras e outras áreas terapêuticas críticas.
📌 Atualização anual
Em 2025, foram avaliadas 61 substâncias ativas adicionais, com a inclusão de nove novos grupos de substâncias. Atualmente, a lista cobre cerca de 75% dos medicamentos autorizados na UE.
Os medicamentos identificados passam a ser prioritários para ações a nível europeu, com foco no reforço das cadeias de abastecimento e na mitigação de riscos de interrupção.
O INFARMED, I.P. acompanhou e contribuiu ativamente para o processo de revisão da lista.
👉 Saiba mais aqui: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12177634
Sistema de Preços de Referência | Aditamento de novos grupos homogéneos (4.º trimestre de 2025)
📢 O INFARMED, I.P. atualizou a lista dos Grupos Homogéneos e dos preços de referência unitários a vigorar no 4.º trimestre de 2025, no âmbito do Sistema de Preços de Referência, conforme circular informativa nº 114/ CD/ 100.20.200.
🗓️ A partir de 1 de novembro de 2025, entra em vigor a deliberação do Conselho Diretivo que aprova os novos Grupos Homogéneos, incluindo a repristinação do GH1219, com o respetivo preço de referência aprovado.
Saiba mais em: https://lnkd.in/dWehAbyg
Atualização importante | INFARMED, I.P.
Foram atualizadas as listas anexas ao Regulamento sobre notificação prévia de transações de medicamentos para o exterior do país:
🔹 Lista de medicamentos com exportação sujeita a notificação prévia pelo distribuidor por grosso ao INFARMED, I.P. (Deliberação n.º 99/CD/2025)
🔹 Lista de medicamentos com exportação temporariamente suspensa, abrangendo medicamentos críticos em rutura em setembro e os fornecidos com autorização de utilização excecional (Deliberação n.º 100/CD/2025)
As listas entram em vigor no dia útil seguinte ao da sua publicação.
Mais informações consulte: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/11749422
Nova Tabela dos Grupos Homogéneos
Foi aprovada a nova tabela dos Grupos Homogéneos e respetivos preços de referência unitários, que entra em vigor a partir de 1 de outubro de 2025, para o 4.º trimestre do ano.
Para mais informações consulte: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/11628522
Atualização de medicamentos com exportação
💊 Foi publicada a Deliberação n.º 96/CD/2025, que atualiza a lista de medicamentos com exportação temporariamente suspensa.
Esta medida visa garantir a normalização do abastecimento dos medicamentos críticos que estiveram em rutura em agosto, bem como daqueles que estão a ser abastecidos com autorização de utilização excecional.
A lista completa está disponível, em formato eletrónico, na área de Gestão da Disponibilidade do Medicamento.
Saiba mais em: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/11603253
Atualização na Comercialização de Medicamentos
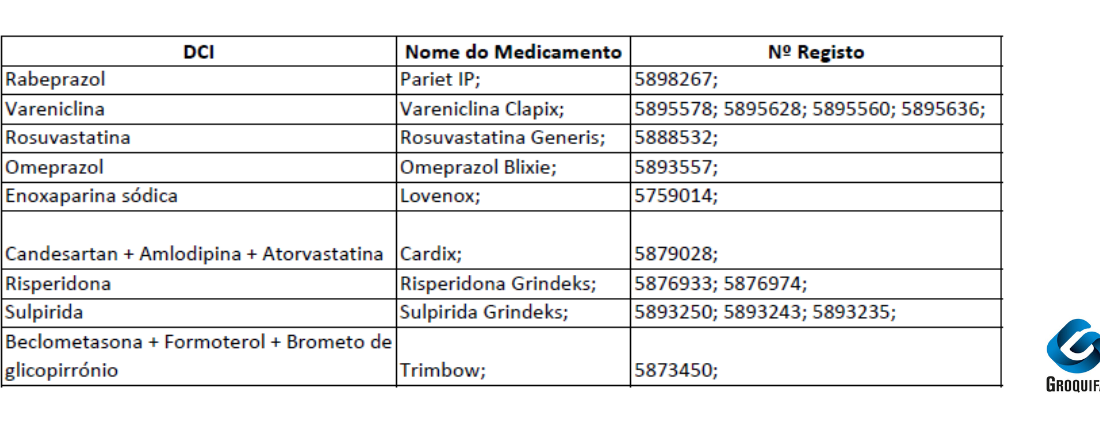
A partir de 1 de agosto de 2025, iniciam-se as alterações na comercialização dos medicamentos comparticipados presentes na imagem acima representada.
– Informa-se também, que decorrente de transferência de comparticipação, existiu uma notificação de início de comercialização dos seguintes medicamentos:
-Bilastina Pharmakern para Bilastina Pharmakern
N.º registo 5816517 para N.º registo 5816525
-Mirtazapina ratiopharm para Mirtazapina refta
N.º registo 5930482 para N.º registo 5860531
N.º registo 5569181 para N.º registo 5860549
-Sertralina Generis para Sertralina Generis Phar
N.º registo 4884680 para N.º registo 5740816
N.º registo 4884888 para N.º registo 5740824
N.º registo 4885182 para N.º registo 5740840
-Omeprazol Blixie para Omeprazol Tecnigen
N.º registo 2978195 para N.º registo 5879341
Para mais informações, consulte os canais oficiais ou a sua farmácia habitual.
Preços de Referência | Novos grupos homogéneos
Já está disponível a atualização da lista de Grupos Homogéneos e dos preços de referência unitários para o 3.º trimestre de 2025.
Consulte a informação completa na área do Sistema de Preços de Referência, incluindo:
–Circular Informativa n.º 082/CD/100.20.200
– Deliberação n.º 076/CD/2025
Mais informações consulte: https://www.infarmed.pt/web/infarmed/entidades/medicamentos-uso-humano/avaliacao-tecnologias-saude/avaliacao-terapeutica-e-economica/sistema-de-precos-de-referencia
Alegações com produtos cosméticos
O INFARMED publicou no passado dia 14 de julho de 2025, a Circular Informativa Nº 085/CD/100.20.200 sobre o Regulamento da Comissão (EU) nº655/2013 que estabelece normas e critérios comuns para a fundamentação de alegações com produtos cosméticos.
Este regulamento tem como objetivo proteger os utilizadores finais de declarações enganosas e permitir-lhes tomar decisões informadas na hora da escolha dos produtos que melhor se adequam às suas necessidades.
Antevendo possíveis constrangimentos na aplicação deste Regulamento, o Infarmed publicou previamente duas circulares informativas: nº106/CD/100.20.200, de 27 de julho de 2018, e a nº097/CD/550.20.00, de 5 de junho de 2019. No entanto, verificou-se a existência de alegações no mercado de produtos cosméticos que violam os critérios de imparcialidade e de tomada de decisão do consumidor.
Atendendo ao acima exposto, devem ser tomadas as seguintes medidas:
-
As entidades (Pessoa Responsável ou Distribuidores) que colocam no mercado nacional produtos cosméticos deverão adotar as medidas consideradas necessárias de forma a repor a conformidade no que respeita às alegações constantes nos produtos que disponibilizam.
-
Na ausência da adoção de medidas corretivas num prazo razoável, serão adotadas as medidas legalmente previstas no Decreto-Lei 23/2025, de 19 de março.
Mais informações consulte: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/11449083