1ª Atualização Anual da Lista de Medicamentos Críticos
Foi publicada a 1ª atualização anual da lista de medicamentos críticos da União Europeia, no passado dia 12 de dezembro de 2025.
A Agência Europeia de Medicamentos (EMA), em articulação com os Chefes das Agências de Medicamentos (HMA) e a Comissão Europeia, publicou este instrumento fundamental para prevenir ruturas de abastecimento e garantir a disponibilidade de medicamentos essenciais na UE, reforçando uma abordagem coordenada e preventiva entre as autoridades reguladoras.
A lista inclui medicamentos de uso humano considerados essenciais para o bom funcionamento dos sistemas de saúde, abrangendo medicamentos inovadores e genéricos, em áreas como vacinas, doenças raras e outras áreas terapêuticas críticas.
📌 Atualização anual
Em 2025, foram avaliadas 61 substâncias ativas adicionais, com a inclusão de nove novos grupos de substâncias. Atualmente, a lista cobre cerca de 75% dos medicamentos autorizados na UE.
Os medicamentos identificados passam a ser prioritários para ações a nível europeu, com foco no reforço das cadeias de abastecimento e na mitigação de riscos de interrupção.
O INFARMED, I.P. acompanhou e contribuiu ativamente para o processo de revisão da lista.
👉 Saiba mais aqui: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12177634
Alteração ao SIATS | Submissão dos novos preços RAP 2026
O SIATS foi otimizado para facilitar a submissão dos novos preços de medicamentos não genéricos e não biossimilares, que entrarão em vigor a 01 de janeiro de 2026.
Assista ao vídeo ilustrativo e veja como a submissão foi simplificada.
Mais informações aqui: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12069668
Atualização na Comercialização de Medicamentos
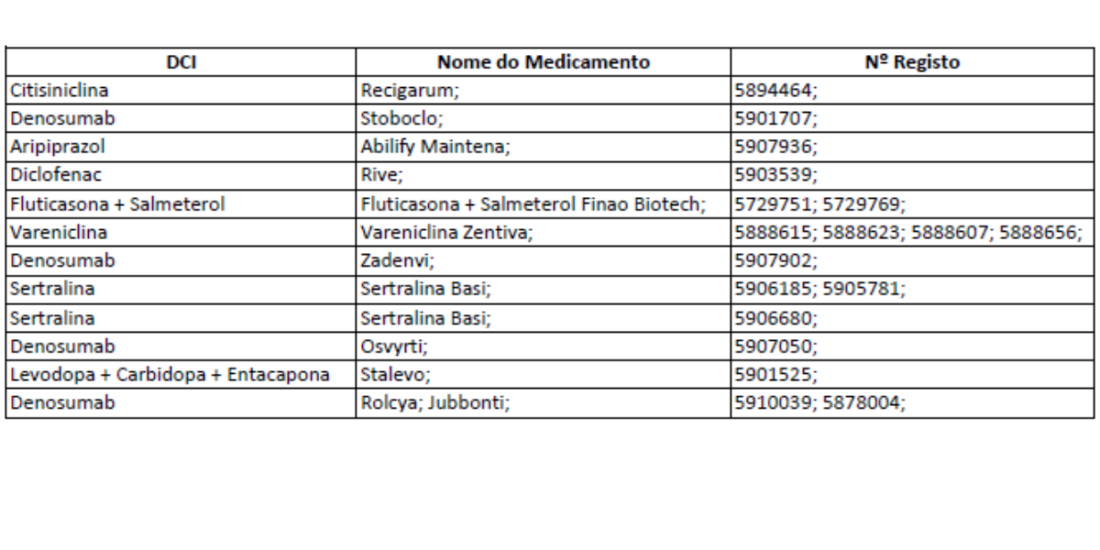
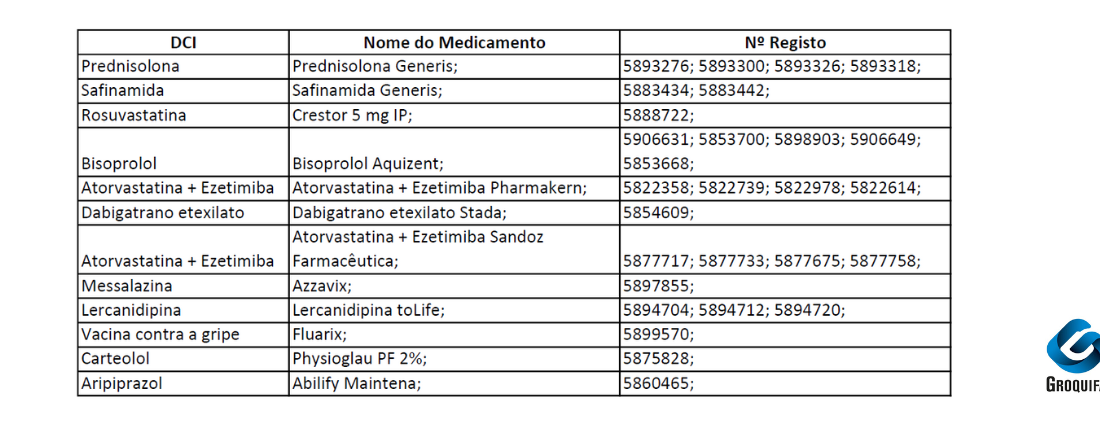
A partir de 1 de dezembro de 2025, inicia-se o início da comercialização dos medicamentos comparticipados presentes na imagem.
– Informa-se também, que decorrente de transferência de comparticipação, existiu uma notificação de início de comercialização dos seguintes medicamentos:
-Twinrix Adulto para Twinrix Adulto
N.º registo 2591683 para N.º registo 2441889
-Atorvastatina Mylan para Atorvastatina Mylan
N.º registo 5434857 para N.º registo 5900105
N.º registo 5434923 para N.º registo 5900121
Para mais informações, consulte os canais oficiais ou a sua farmácia habitual.
Atualização da lista de medicamentos com exportação temporariamente suspensa
Atualização da lista de medicamentos com exportação temporariamente suspensa
Foi publicada a Circular Informativa n.º 129/CD/100.20.200 de 07/11/2025, que divulga a Deliberação n.º 113/CD/2025, a qual atualiza a lista de medicamentos cuja exportação se encontra temporariamente suspensa.
Esta medida tem como objetivo assegurar a normalização do abastecimento dos medicamentos críticos que estiveram em rutura durante o mês de outubro, bem como dos medicamentos que estão a ser fornecidos ao abrigo de autorizações de utilização excecional.
A lista eletrónica atualizada está disponível na área Gestão da disponibilidade do medicamento.~
Saiba mais em: Atualização da lista de medicamentos cuja exportação é temporariamente suspensa | novembro de 2025 – INFARMED, I.P.
Sistema de Preços de Referência | Aditamento de novos grupos homogéneos (4.º trimestre de 2025)
📢 O INFARMED, I.P. atualizou a lista dos Grupos Homogéneos e dos preços de referência unitários a vigorar no 4.º trimestre de 2025, no âmbito do Sistema de Preços de Referência, conforme circular informativa nº 114/ CD/ 100.20.200.
🗓️ A partir de 1 de novembro de 2025, entra em vigor a deliberação do Conselho Diretivo que aprova os novos Grupos Homogéneos, incluindo a repristinação do GH1219, com o respetivo preço de referência aprovado.
Saiba mais em: https://lnkd.in/dWehAbyg
Atualização importante | INFARMED, I.P.
Foram atualizadas as listas anexas ao Regulamento sobre notificação prévia de transações de medicamentos para o exterior do país:
🔹 Lista de medicamentos com exportação sujeita a notificação prévia pelo distribuidor por grosso ao INFARMED, I.P. (Deliberação n.º 99/CD/2025)
🔹 Lista de medicamentos com exportação temporariamente suspensa, abrangendo medicamentos críticos em rutura em setembro e os fornecidos com autorização de utilização excecional (Deliberação n.º 100/CD/2025)
As listas entram em vigor no dia útil seguinte ao da sua publicação.
Mais informações consulte: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/11749422
Atualização na Comercialização de Medicamentos
📢 Atualização na Comercialização de Medicamentos
A partir de 1 de outubro de 2025, inicia-se o início da comercialização dos medicamentos comparticipados presentes na imagem.
– Informa-se também, que decorrente de transferência de comparticipação, existiu uma notificação de início de comercialização dos seguintes medicamentos:
– Ramipril Sandoz para Ramipril Sandoz
N.º registo 5667183 para N.º registo 5602669
N.º registo 5667381 para N.º registo 5602677
N.º registo 5666987 para N.º registo 5602701
– Clopidogrel Kaissan para Clopidogrel Mesiproc
N.º registo 5207550 para N.º registo 5267414
– Atorvastatina Ratiopharm para Atorvastatina Refta
N.º registo 5416649 para N.º registo 5889340
N.º registo 5416664 para N.º registo 5889373
N.º registo 5416714 para N.º registo 5889423
– Celecoxib Ratiopharm para Celecoxib Refta
N.º registo 5487053 para N.º registo 5895859
N.º registo 5487061 para N.º registo 5895867
– Fluoxetina Generis Phar para Fluoxetina Generis
N.º registo 3653680 para N.º registo 5730270
N.º registo 4582284 para N.º registo 5730304
– Clopidogrel Generis Phar para Clopidogrel Aurobindo
N.º registo 5209408 para N.º registo 5727615
Para mais informações, consulte os canais oficiais ou a sua farmácia habitual.
.
#Groquifar #Medicamentos #Saúde #Farmacêutica
Nova Tabela dos Grupos Homogéneos
Foi aprovada a nova tabela dos Grupos Homogéneos e respetivos preços de referência unitários, que entra em vigor a partir de 1 de outubro de 2025, para o 4.º trimestre do ano.
Para mais informações consulte: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/11628522
Campanha de Vacinação Sazonal 2025/2026
É já no próximo dia 23 de setembro, que a Campanha de Vacinação Sazonal 2025/2026 contra a Gripe e a Covid-19, começa!
📍Novidade importante:
A vacinação contra a gripe passa a ser gratuita para todas as crianças entre os 6 e os 23 meses de idade, uma faixa etária com níveis de hospitalização semelhantes aos registados em pessoas idosas. A DGS recomenda também a vacinação de crianças entre os 2 e os 4 anos.
Reforçando o seu compromisso com a saúde pública, a GROQUIFAR volta a integrar o grupo de trabalho da campanha de vacinação sazonal, sob coordenação da Direção Executiva do Serviço Nacional de Saúde (DE-SNS), contribuindo ativamente para o sucesso da iniciativa.
Atualização de medicamentos com exportação
💊 Foi publicada a Deliberação n.º 96/CD/2025, que atualiza a lista de medicamentos com exportação temporariamente suspensa.
Esta medida visa garantir a normalização do abastecimento dos medicamentos críticos que estiveram em rutura em agosto, bem como daqueles que estão a ser abastecidos com autorização de utilização excecional.
A lista completa está disponível, em formato eletrónico, na área de Gestão da Disponibilidade do Medicamento.
Saiba mais em: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/11603253