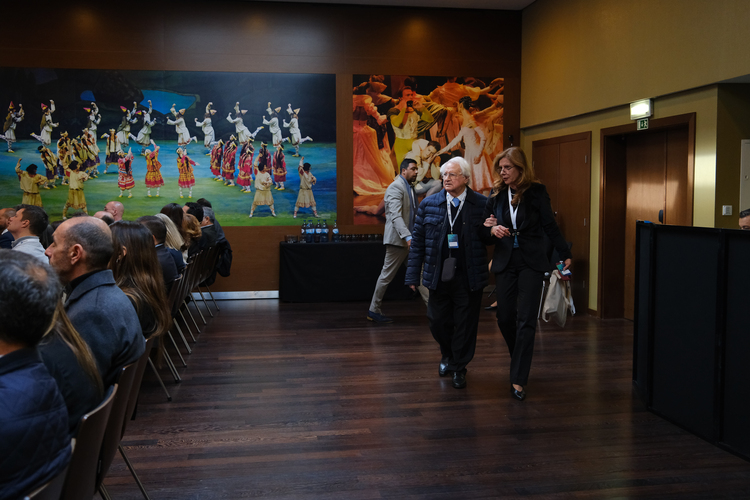Melhores Momentos_Congresso 6 de março
O Congresso da Groquifar foi, mais uma vez, um momento de encontro, partilha e fortalecimento das relações entre associados, parceiros e profissionais do setor. Ao longo do evento, tivemos a oportunidade de assistir a intervenções inspiradoras, trocar experiências e refletir sobre os desafios e oportunidades que marcam o presente e o futuro da nossa atividade.
Para recordar os melhores momentos vividos durante o congresso, disponibilizamos uma galeria de fotografias que captam a essência deste encontro. Reviva o ambiente, os sorrisos e os destaques que fizeram deste evento um verdadeiro sucesso.
👉 Aceda aqui à galeria de fotografias aqui: Groquifar 50 Anos, de Stream Dream – Imagem e Comunicação
Congresso 50 ANOS DE HISTÓRIA Groquifar
Congresso 50 Anos Groquifar
🎉O Congresso dos 50 anos da 𝐆𝐫𝐨𝐪𝐮𝐢𝐟𝐚𝐫 ficará, sem dúvida, na nossa história.
No passado dia 𝟔 𝐝𝐞 𝐦𝐚𝐫ç𝐨, reunimos 𝐚𝐬𝐬𝐨𝐜𝐢𝐚𝐝𝐨𝐬, 𝐩𝐚𝐫𝐜𝐞𝐢𝐫𝐨𝐬 𝐞 𝐜𝐨𝐧𝐯𝐢𝐝𝐚𝐝𝐨𝐬 num evento muito especial que assinalou meio século de história da Groquifar.
Ao longo do dia, partilhámos 𝐜𝐨𝐧𝐡𝐞𝐜𝐢𝐦𝐞𝐧𝐭𝐨 𝐞 𝐫𝐞𝐟𝐥𝐞𝐱𝐚̃𝐨 através de várias apresentações que abordaram temas transversais, como 𝐢𝐧𝐭𝐞𝐥𝐢𝐠𝐞̂𝐧𝐜𝐢𝐚 𝐚𝐫𝐭𝐢𝐟𝐢𝐜𝐢𝐚𝐥 e 𝐬𝐮𝐬𝐭𝐞𝐧𝐭𝐚𝐛𝐢𝐥𝐢𝐝𝐚𝐝𝐞, mas também desafios e perspetivas específicas das diferentes áreas de atividade representadas na associação.
O dia terminou com um 𝐉𝐚𝐧𝐭𝐚𝐫 𝐝𝐞 𝐆𝐚𝐥𝐚, um momento de celebração e reconhecimento, onde tivemos a oportunidade de homenagear os 𝐚𝐬𝐬𝐨𝐜𝐢𝐚𝐝𝐨𝐬 𝐦𝐚𝐢𝐬 𝐚𝐧𝐭𝐢𝐠𝐨𝐬 𝐝𝐞 𝐜𝐚𝐝𝐚 𝐝𝐢𝐯𝐢𝐬𝐚̃𝐨, destacando o seu percurso e contributo para o crescimento e fortalecimento da Groquifar ao longo dos anos.
Deixamos um 𝐚𝐠𝐫𝐚𝐝𝐞𝐜𝐢𝐦𝐞𝐧𝐭𝐨 𝐬𝐢𝐧𝐜𝐞𝐫𝐨 a todos os participantes, cuja presença tornou este encontro ainda mais significativo, e também aos 𝐧𝐨𝐬𝐬𝐨𝐬 𝐩𝐚𝐭𝐫𝐨𝐜𝐢𝐧𝐚𝐝𝐨𝐫𝐞𝐬, cujo apoio foi fundamental para tornar possível este evento.
👏 A todos os que fizeram parte deste dia: 𝐦𝐮𝐢𝐭𝐨 𝐨𝐛𝐫𝐢𝐠𝐚𝐝𝐚 𝐩𝐨𝐫 𝐜𝐞𝐥𝐞𝐛𝐫𝐚𝐫𝐞𝐦 𝐜𝐨𝐧𝐧𝐨𝐬𝐜𝐨 𝐞𝐬𝐭𝐞𝐬 𝟱𝟎 𝐚𝐧𝐨𝐬 𝐝𝐞 𝐡𝐢𝐬𝐭𝐨́𝐫𝐢𝐚!
Atualização – Sistema de Preços de Referência | 1.º trimestre 2026
Foram atualizados os Grupos Homogéneos e os preços de referência unitários para o 1.º trimestre de 2026.
Consulte a Circular Informativa N.º 014/CD/100.20.200 (09/02/2026) e a Deliberação N.º 009/CD/2026 (05/02/2026) na área do Sistema de Preços de Referência.
Saiba mais em: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12472236
Atualização – fevereiro 2026
🚨 Foi atualizada a lista de medicamentos com exportação temporariamente suspensa (Deliberação n.º 008/CD/2026), com o objetivo de normalizar o abastecimento de medicamentos críticos em rutura, medicamentos ao abrigo de autorização de utilização excecional e todos os que contêm quetiapina.
A lista está disponível na área de Gestão da Disponibilidade do Medicamento: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12472433
Despacho nº40/G/2026 – Aquisição de PF possível com cartão antigo + certificado de formação
A Groquifar – Associação de Grossistas de Produtos Químicos e Farmacêuticos tem atuado com sentido de responsabilidade e liderança setorial para defender as empresas de distribuição e os seus profissionais. Diante das dificuldades na frequência atempada das ações de formação e na emissão do APF, a associação desenvolveu diligências junto das entidades competentes, garantindo uma solução célere, juridicamente sustentada e operacionalmente viável.
👉 Com a publicação do Despacho n.º 40/G/2026 da DGAV é agora possível que, até ao final de 2026, adquirir produtos fitofarmacêuticos com a apresentação do cartão de aplicador antigo + certificado de formação. Esta medida assegura a continuidade da atividade das empresas, protege os Técnicos Responsáveis e Operadores de Venda e reforça a estabilidade jurídica do setor.
Saiba mais aqui: https://diariodarepublica.pt/dr/detalhe/decreto-lei/40-2026-1049254412
Atualização de listas de medicamentos | janeiro 2026
O INFARMED, I.P. atualizou as listas do Regulamento sobre a notificação prévia de transações de medicamentos para o exterior do país.
Inclui:
• Medicamentos sujeitos a notificação prévia para exportação/distribuição na UE
• Medicamentos com exportação temporariamente suspensa (críticos, AUE e quetiapina)
Em vigor no dia útil seguinte à publicação.
Plataforma SiExp será atualizada.
 Saiba mais em: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12307601
Saiba mais em: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12307601
A Groquifar marcou presença no passado dia 15 de janeiro de 2026, na sessão comemorativa dos 33 anos do INFARMED, I.P., integrada na Reunião Extraordinária do Conselho Consultivo.
Uma sessão que ficou marcada pela apresentação do novo Conselho Diretivo e pela partilha das linhas estratégicas do Infarmed para 2026, onde temas como sustentabilidade, inovação, transformação digital e modernização da regulação, estiveram no centro da discussão.
Um momento de partilha e de reforço da cooperação entre os vários agentes do setor da saúde.
Saiba mais em: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12332849
A lista dos Grupos Homogéneos e dos preços de referência unitários a vigorar no 1.º trimestre de 2026 foi aprovada e entra em vigor a 1 de janeiro de 2026.
Saiba mais em: https://www.infarmed.pt/web/infarmed/infarmed/-/journal_content/56/15786/12237933
Nova plataforma SIOMS
O INFARMED lança funcionalidades que permitem solicitar, pagar e emitir certificados e declarações de medicamentos de forma automática.
–Registo obrigatório a partir de 22/12/2025
–Pedidos disponíveis a partir de 30/01/2026
Registe-se: https://extranet.infarmed.pt/SIOMS-fo
Documentos assinados com selo eletrónico qualificado e códigos de verificação únicos para maior segurança e fiabilidade.